Introducción
La diabetes cuenta entre sus complicaciones más temidas a la úlcera de pie diabético (UPD), la cual contribuye con el 80 % de todas las amputaciones no traumáticas de miembros inferiores a nivel mundial1. Los factores de crecimiento (FC) desempeñan un papel fundamental al inicio y durante las diferentes fases de la cicatrización. Factores como el FCE, el factor de crecimiento del endotelio vascular (VEGF), el factor de crecimiento transformante beta (TGF-β), el factor de crecimiento plaquetario (PDGF), el factor de crecimiento fibroblasto básico (FGF), el factor de crecimiento celular epitelial (ECGF), el factor de necrosis tumoral (TNF-α) y la interleuquina 6 (IL-6) están notablemente disminuidos. Esto provoca un desbalance entre la formación y la degradación de la matriz extracelular (MEC) en un contexto caracterizado por un exceso de citoquinas inflamatorias, especies reactivas de oxígeno, productos avanzados de glicación, proteasas de la matriz extracelular y una biopelícula poli microbiana. La senescencia celular y la disfunción molecular promueven una ulcera crónica2,3, donde la reducción del FCE, y el descenso de la actividad tirosina quinasa de su receptor específico, el Epidermal Growth Factor Receptor (FCER), juega un papel preponderante4.
Los niveles de FCE en plasma no son detectables, pero las plaquetas contienen niveles mesurables. Después de la coagulación, las concentraciones de FCE son suficientes para inducir mitosis y migración celular. Regula el crecimiento, la diferenciación y el metabolismo de varias células, sirviendo como un mitógeno y quimioatrayente para neutrófilos y monocitos, estimulando la migración de fibroblastos y permitiendo la síntesis y depósito de colágeno. A su vez, logra efectos antiinflamatorios, con beneficio para controlar la respuesta inflamatoria excesiva presente en las UPD. De igual forma, estimula la producción de células endoteliales y epiteliales5.
Los tratamientos tradicionales de la UPD incluyen el control de la glucosa en sangre, el tratamiento de la infección e insuficiencia vascular, la eliminación del tejido muerto y el uso de apósitos y vendajes especiales. Sin embargo, la cicatrización de estas úlceras puede ser un proceso largo y costoso. Implementar nuevas tecnologías para facilitar la cicatrización requiere de un respaldo de pruebas con alta calidad de evidencia sobre su eficacia y coste-efectividad. En este sentido, el Grupo Internacional de Trabajo de Pie Diabético6 (IWGDF) recomienda como tratamientos complementarios el uso de apósitos de octasulfato de sacarosa, terapias de presión negativa para heridas quirúrgicas, el uso de productos derivados de la placenta, parches autólogos de leucocitos/plaquetas/fibrina, el uso de oxigenoterapia tópica y oxígeno hiperbárico. Las terapias con FC como tratamiento complementario no han sido recomendadas, si bien su utilización en entornos clínicos de investigación ha mostrado datos alentadores en la mejora de la cicatrizacion7. El impacto del uso de FCE sobre el riesgo de amputación, en comparación con cualquier otro factor de crecimiento, placebo o atención estándar, no ha mostrado diferencias significativas. Sin embargo, la cicatrización completa de las úlceras ocurre con mayor probabilidad y en menor tiempo8. El FCE está clínicamente disponible, en formulaciones para aplicación intralesional y tópica. Los resultados de estudios clínicos han sido prometedores, mostrando una aceleración en el proceso de cicatrización y reducción de estancia hospitalaria9–13. El rhFCE, fue desarrollado por el Centro de Ingeniería Genética y Biotecnología de Cuba, aprobado para su uso en el año 200614 y luego registrado en países de Latinoamérica, Euro Asia y África. No ha sido registrado en agencias internacionales como la Administración de Alimentos y Medicamentos de los EE.UU. (FDA) ni en la Agencia Europea de Medicamentos (EMA). En Uruguay, el rhFCE (Heberprot-P) está disponible en el Formulario Terapéutico de Medicamentos del Ministerio de Salud Pública desde el año 2009.
Nuestro objetivo es comunicar la experiencia obtenida con uso de rhFCE como tratamiento complementario de la UPD en la Unidad de Pie del Hospital Público.
Utilizamos como variables de respuesta al tratamiento el porcentaje de reducción del área de la úlcera en un plazo de 8 semanas y el cierre total de la lesión. También se valoraron los efectos adversos.
Material y métodos
Estudio observacional de vida real, descriptivo, retrospectivo. Se recabaron datos del registro de la historia clínica protocolizada de 5 pacientes diabéticos mayores de 18 años con úlceras neuroisquémicas del pie de al menos 4 semanas de evolución, con un diámetro mayor a 1 cm2, tratadas con rhFCE intradérmico entre junio y diciembre de 2022.
Se obtuvo información sobre: demografía, antecedentes del control glucémico, comorbilidades, características de la lesión y variables relacionadas al resultado del uso del fármaco, tales como: área de la úlcera pre y post tratamiento, porcentaje de reducción del área de la lesión, cierre de la úlcera, efectos secundarios, número de aplicaciones, días de tratamiento.
Previo al uso de rhFCE, e evaluó y trató la perfusión vascular y cualquier proceso infeccioso. Todos los pacientes recibieron además un cuidado estándar de la úlcera basado en: lavado con suero salino al 0,9% (SF), desbridado con bisturí y retiro del tejido desvitalizado, cura con gasa embebida en SF y apósito de gasa.
Una vez que el paciente dio su consentimiento informado autorizando el tratamiento, el producto se aplicó de forma intradérmica posterior al desbridado de la herida. Se aplicaron 75 μg de rhFCE (reconstituidos en 4 cc de agua destilada) con una jeringa de 5 cc, en el contorno interno de la lesión y fondo de la herida para asegurar una distribución uniforme, cambiando la aguja (N°26 G x 1/2) para cada punción. Finalmente, se colocó una gasa embebida con SF y se realizó una compactación suave con apósito de gasa para absorber cualquier descarga. En domicilio, se realizó curaciones diarias con SF.
El rhFCE se aplicó semanalmente; su frecuencia fue determinada por el médico tratante, según la condición clínica de la herida (área, profundidad) y las comorbilidades del paciente (cardiopatía, insuficiencia renal) (ver tablas 1 y 2, gráfico 2). La fase de tratamiento comprendió desde la primera administración del rhFCE el día uno y finalizó cuando ocurrió el cierre de la lesión, una úlcera ≤ 1 cm2 o reducción del área mayor al 75%, con un tejido de granulación efectivo definido como: presencia de formaciones granulares miliares rojizas, difusas, dispersas y lustrosas que sangran con facilidad después de la manipulación. La presencia del tejido epitelial sin secreción cubriendo la úlcera constituyó una curación completa. Los controles de la herida fueron semanales, midiendo el área de la úlcera con un calibre. El porcentaje de reducción del área se calculó con la fórmula: (diámetro inicial - diámetro final) / diámetro inicial x 100. Luego de finalizado el tratamiento los pacientes continuaron en control cada 3 meses durante un año, evaluando posibles recidivas.
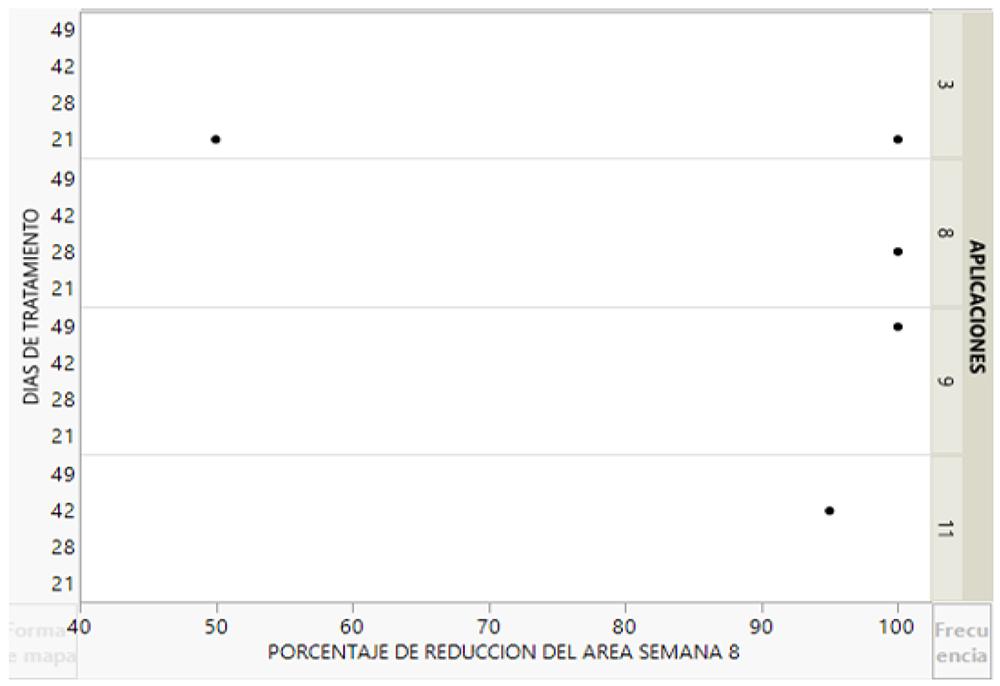
Gráfico 2. Porcentaje de reducción del área en la semana 8 vs número de aplicaciones -días de tratamiento.Número de aplicaciones: M: 8; ±3,2. Días de tratamiento: M: 32,2 (R 21-49).
Tabla 1. Características de los pacientes.

HbA1c: hemoglobina glicosilada. Texas: Clasificación de Texas15. UQ: ulcera quirúrgica. UP ulcera por presión.
Los datos recopilados se analizaron con el software JMP Trial 18.0.1 (análisis de datos) Inc. 2024, versión 18.01. Las variables cualitativas se presentan como frecuencias absolutas y porcentajes. Para las variables cuantitativas se aplicó estadística descriptiva, medidas de resumen central y de dispersión (media, desviación estándar e intervalos de confianza con 95% de confiabilidad) con el método binomial.
Se aplicó rhFCE a 4 pacientes con DM2 y 1 con DM1. Predominó el sexo masculino (3/5). La media de edad fue de 57,8 años (DE: 13,9; rango: 40 a 75 años). Dos pacientes presentaron como comorbilidades cardiopatía isquémica estable e IRC, uno de ellos estaba en tratamiento dialítico. El control glucémico mostró una media de HbA1c de 7,8% (DE: 0,8; rango: 6,7 – 8,8). Según la etiología de la lesión, se presentaron 3 úlceras secundarias a amputación y 4 úlceras por presión (1 paciente presentó 3 lesiones simultáneas, figura 1, paciente 3).
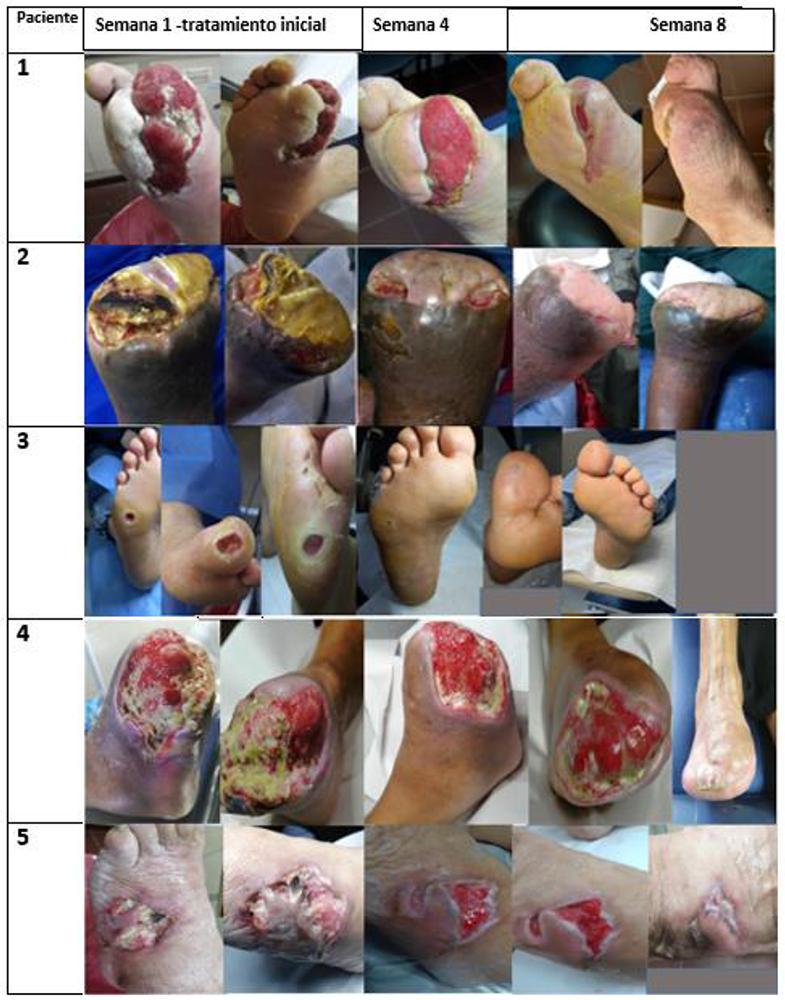
Figura 1. Pacientes representativos. Evolución clínica.1. Masculino. 43 años. DM1. Amputacion en rayo de hallux. Epitelización.2. Masculino. 72 años. Cardiopatía isquémica estable e IRC. Epitelización.3. Masculino. 43 años. Tres lesiones simultáneas. Epitelización.4. Femenino. 62 años. Hemodiálisis. Reducción del área 50%. Epitelización al sexto mes.5. Femenino. 69 años. Reposicionamiento del colgajo. Epitelización.
Las úlceras se caracterizaron según la clasificación de Texas15 como: II A (2 pacientes), IIIA (1 paciente), IIC (1 paciente), IIIC (1 paciente). Estas presentaban una media de retraso en la cicatrización de 90 días (DE: 63,6) antes del inicio del tratamiento. Las características de los pacientes se describen en la tabla 1.
Resultados
La media del área inicial para todos los pacientes fue de 38cm2, (DE: 25,1; rango: 8-80). Al final de las 8 semanas, la media del área fue de 8,2 cm2 (DE: 15; rango: 40) (Tabla 2). En la valoración del resultado, observamos una media de reducción del área de la lesión del 54,4% (DE: 23,3; rango: 25-97) a las 4 semanas, y del 89% (DE: 19,5; rango: 50-100) a las 8 semanas (Gráfico 1 A-B). Finalmente, la cicatrización completa ocurrió en los 4 pacientes en un promedio de 56 a 60 días, y en 1 paciente a los 6 meses. Este último paciente logró un tejido de granulación efectivo con una reducción del 50% del área de una lesión neuroisquémica de 80 cm2, y recibió 1 aplicación semanal debido a su condición de IRC en hemodiálisis. (Figura 1, paciente 4). La respuesta clínica evolutiva de todos los pacientes se muestra en la figura 1.
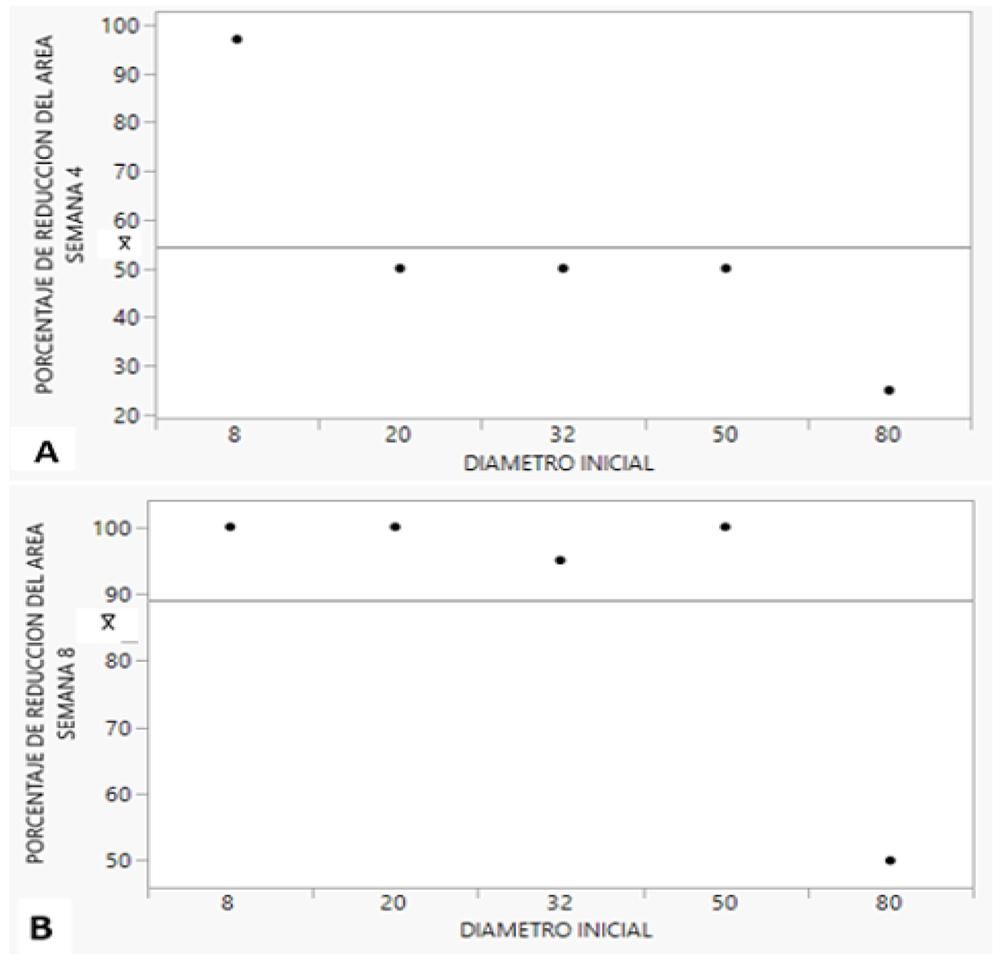
Gráfico 1. Análisis univariante de porcentaje de reducción del área con respecto al diámetro inicial.A: semana 4. Ⴟ: media 54,4% ± 19,5.B: semana 8. Ⴟ: media 89% ± 23,3.
De acuerdo a la posología del producto, el rhFCE se indica hasta un máximo de 24 aplicaciones, con una media de 10 a 12 aplicaciones. En nuestra observación, se realizó una media de 8 aplicaciones (DE: 3,2; rango: 3-11) por paciente durante un promedio de 32,2 días (rango: 21-49) de tratamiento (Tabla 2). Los pacientes 4 y 5 recibieron 1 aplicación semanal en tres ocasiones; en un caso, por su condición de IRC (en hemodiálisis), y en el otro, el reposicionamiento de un colgajo de piel tras la granulación del lecho aceleró el proceso de cicatrización (Figura 1).
Como efectos secundarios, se documentó dolor en el sitio de punción de breve duración durante la aplicación del producto en 3 pacientes, y escalofríos en 2 de ellos. En resumen, la epitelización ocurrió en 6 de las 7 úlceras luego de 8 semanas de iniciado el tratamiento. Posteriormente, el seguimiento se realizó cada 3 meses durante un año, sin que se presentaran recidivas.
Discusión
La selección de una estrategia de cicatrización adecuada es prioritaria para el éxito; esta debería promover un cierre rápido y completo de la lesión, lo que contribuye a disminuir el tiempo de úlcera abierta y, con ello, la posibilidad de complicaciones. El complejo activado FCE-FCER promueve cambios génicos, con una respuesta bioquímica celular que regula la inflamación, la proliferación fibroblástica, la migración celular, la angiogénesis y la contracción de la herida, sugiriendo que es una estrategia útil para la curación de heridas16,8,17.
La implementación del uso de rhFCE en nuestros pacientes logró, a las 8 semanas, una respuesta efectiva con porcentaje de reducción del área de la lesión del 89%, y luego un cierre total de la úlcera en 4 de ellos (Figura 1). Cabe destacar que las úlceras tratadas fueron neuropáticas e isquémicas de grados II y III según la clasificación de Texas, con más de 30 cm2 de área promedio. Fueron necesarias 8 aplicaciones promedio por paciente, en un tiempo medio de 32 días, sin que se registraran eventos adversos significativos (Tabla 2, Gráfico 2). Las diferentes características de los pacientes y de las úlceras influyeron en la cicatrización; sin embargo, la respuesta fue homogénea y se logró tejido de granulación con reducción del área en un promedio de 4 semanas, seguido de la cicatrización en la mayoría de los casos a las 8 semanas (Gráfico 1, Figura 1). Aun en el paciente cuya cicatrización completa ocurrió posterior al periodo de tratamiento, se obtuvieron mejoras significativas en la granulación a las 8 semanas (Figura 1, paciente 4).
No se presentaron recidivas durante más de un año en el seguimiento de estos pacientes. La observación realizada sobre la respuesta al rhFCE en esta experiencia se alinea con aquellos trabajos que informan la ocurrencia de una cicatrización total en plazos similares18,19 y cuya efectividad se mantiene con diferentes dosis de rhFCE20. Es importante tener en cuenta que tres de los cinco pacientes experimentaron efectos colaterales. Aunque fueron efectos relativamente leves en comparación con el beneficio de la cicatrización, la gestión de los mismos garantiza la comodidad y seguridad de los pacientes21.
La respuesta al rhFCE es mayor si se aplica en la matriz extracelular profunda de la herida, pero el dolor en el lugar de la inyección es una queja común22. Reportes de vigilancia activa de la administración de factor de hrFCE confirman el perfil clínico beneficioso y seguro del tratamiento21. Aun siendo el FCE un potente mitógeno, el tratamiento no ha mostrado transformaciones malignas en las células16,23.
Junto a medidas de cuidado local, el uso de rhFCE podría promover un perfil de cicatrización beneficioso con impacto positivo en la prevención de futuras úlceras. Diversas publicaciones refieren un 5% de recaídas por año con el uso de rhFCE20, y en úlceras postquirúrgicas se ha reportado una tasa de recurrencia menor cuando se aplica el rhFCE24.
Los costos del uso de nuevas tecnologías en cicatrización puede significar una dificultad a la hora de su implementación; sin embargo, los estudios señalan que acortar el tiempo de la ulcera abierta siempre es eficiente, ofreciendo la posibilidad de cicatrización y una mejora en la calidad de vida de los pacientes25–28. En la Unidad de Pie, los estudios de costos del tratamiento de la UPD muestran una carga económica notable, con un gasto promedio de 8.799 dólares por paciente (2022) para un periodo de ulcera tratada de 12 semanas29.
Si bien esta observación muestra resultados prometedores en nuestros pacientes, la misma se ve limitada por el número pequeño de pacientes y por tratarse de un análisis retrospectivo, sin grupo control.
















