Introducción
Las enfermedades autoinmunes sistémicas (EAS) son trastornos que generan una alteración en la inmunidad tanto humoral como celular. Se ha descrito déficit del complemento, asplenia funcional, alteraciones del sistema fagocítico así como déficit en la actividad de los linfocitos T citotóxicos y alteración en la función de las células T supresoras como parte del proceso de la enfermedad.1-3
El tratamiento de estas patologías se basa en terapia inmunosupresora a largo plazo; entre ellas los corticoides bloquean la proliferación de células T así como su actividad microbicida, lo que compromete la respuesta inmune antígeno especifica aumentando así el riesgo de infección por patógenos oportunistas y típicos.1)(2
Las infecciones ocupan un lugar importante dentro de la morbimortalidad (30% en regiones de mayor prevalencia) 3. Dentro de estas infecciones, destacamos la tuberculosis, enfermedad infecciosa re- emergente, causada por Mycobacterium tuberculosis - bacilo acido alcohol resistente (BAAR), patógeno aerobio estricto intracelular. Endémica y con incidencia en ascenso en nuestro medio (25/100.000 hab/año) situando a nuestro país como zona de incidencia intermedia a nivel internacional 4.
En cuanto a la forma de presentación clínica, las extrapulmonares son mas frecuentes en este grupo de pacientes, siendo dificultoso discernir entre infección y actividad de la enfermedad de base. La utilización de técnicas de biología molecular, como reacción en cadena de la polimerasa (PCR GeneXpert) constituye una herramienta de utilidad para definir esta situación.
El correcto y precoz diagnostico tiene implicancias pronosticas así como terapéuticas. El control, seguimiento así como tratamiento de estos pacientes es llevado a cabo por la Comisión Honoraria para la Lucha Antituberculosa y Enfermedades Prevalentes (CHLA-EP). 4
La prevalencia de tuberculosis (TBC) en pacientes con EAS bajo tratamiento inmunosupresor es variable, según el país que reporta las mismas. Dos estudios españoles de pacientes con lupus eritematoso sistémico (LES) refieren una incidencia de 187 casos/100.000 y 153 casos/100.000 (1) ; mientras que un estudio de Filipinas que incluyó 390 pacientes con LES encontraron una incidencia de 13,8% de TBC activa, 74% de ellos presentaban únicamente compromiso pulmonar, destacando que los pacientes con infección diseminada eran los que tenían mayor índice de actividad y agresividad de su EAS, sin relación con la dosis de corticoides recibida al momento del diagnóstico. 1
En otro estudio retrospectivo que incluía a 283 pacientes con LES y 284 con artritis reumatoide (AR) procedentes de Corea, se halló que la afectación tuberculosa más frecuente era pulmonar y predominantemente en pacientes con LES con mayores dosis de corticoides.1)(5
No contamos con datos disponibles en nuestro medio sobre la incidencia de TBC en este grupo de pacientes.
Objetivo
Presentar tres casos clínicos de pacientes con EAS en actividad bajo tratamiento inmunosupresor que presentaron como complicación infecciosa el desarrollo de tuberculosis.
Actualizar la asociación entre EAS y TBC
Caso Clínico 1
Sexo femenino, 23 años. Antecedentes Personales (AP): LES (compromiso cutáneo, articular y hematológico) en tratamiento con prednisona 40 mg/día vía oral en los últimos 6 meses.
Consulta por cuadro de 4 semanas de evolución dado por alteraciones neuropsíquicas, cambios conductuales, cefalea holocraneana y dos episodios de convulsiones tónico-clónico generalizadas, sin elementos de actividad infecciosa. Del examen físico destacamos: Apirética. PM: Anemia clínica, áreas de alopecia en cuero cabelludo con lesión ulcerada de borde eritematoso (Figura 1). SNM: tendencia al sueño, bradipsíquica. Sin alteraciones de los pares craneanos, sector espinal, coordinación, sin rigidez de nuca.

Figura 1: Caso clínico 1: áreas de alopecia en cuero cabelludo, presentando lesión ulcerada redondeada de bordes eritematosos.
De la paraclínica inicial se destaca : Anticuerpos antinucleares (ANA) > 1/640 patrón homogéneo. Anticuerpos anti- DNA, Anti Smith, Anti RO y Anti LA positivos. Hipocomplementemia. VES 120 mm3 Hemograma: Hemoglobina 9,0 gr/dl, Plaquetas 93.000/ mm3 Linfocitos 450/mm3.
Con planteo inicial LES en actividad severa por las manifestaciones neuropisquiátricas se comienza tratamiento con corticoides a altas dosis y se completa valoración neurológica.
TAC de cráneo con y sin contraste: sin lesiones. Angio- RNM: discreta alteración de la señal encefálica bilateral en T2 y FLAIR (Figura 2). Estudio de líquido cefalorraquídeo: aspecto claro, pandy ++, glucosa 0.87 mg/dl, proteínas 1,74 g/dl. Glóbulos blancos: 14/mm3. Cultivo bacteriológico del líquido sin desarrollo. PCR para grupo herpes virus negativo. VDRL negativo. PCR en tiempo real para Mycobacterium tuberculosis positiva.
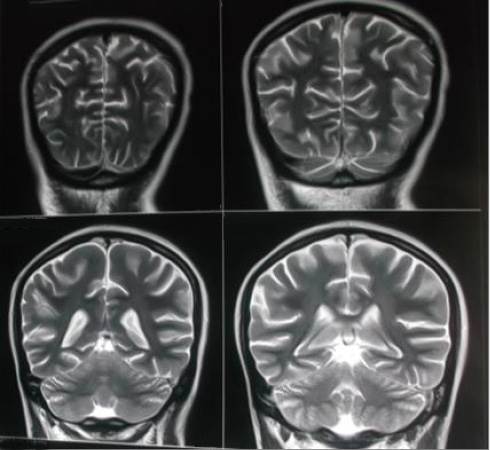
Figura 2: Caso clínico 1: Angio- RNM evidencia discreta alteración de la señal encefálica bilateral en T2 y FLAIR.
Con planteo de meningoencefalitis tuberculosa en paciente cursando empuje severo de LES se inicia tratamiento antibiótico especifico (rifampicina, pirazinamida, isoniacida y etambutol), manteniendo corticoides a dosis de 60mg v/o día.
Evolución clínica favorable con retroceso de las manifestaciones neurológicas y remisión progresiva de los parámetros de actividad. Como complicación presenta hepatitis toxica secundaria al tratamiento antituberculoso, que remite tras suspensión transitoria del mismo iniciando posteriormente con drogas de segunda línea (estreptomicina, etambutol y levofloxacina) durante 12 meses.
En tratamiento actual con hidroxicloroquina, calcio, vitamina D y plan de descenso de corticoides.
Caso Clínico 2
Sexo femenino, 52 años. AP: Hipertensión arterial, obesa.
Consulta por cuadro de dos meses de evolución dado por fiebre sin foco clínico evidente, astenia, adinamia y artromialgias. En la evolución agrega hemoptisis moderada y disnea. Del examen físico destacamos: apirética. PM: normocoloreadas. PP: FR 30 rpm, sin tirajes. Estertores crepitantes en dos tercios inferiores bilaterales.
De la paraclínica se destaca: VES 110/mm3. PCR 70. Hemoglobina 8,2 gr/dl. ANA negativo, ANCA + PR3 173 (VN < 20). Hemocultivos, urocultivo, baciloscopias y cultivo de expectoración: sin desarrollo.
Radiografía de tórax: infiltrado intersticial bilateral y difuso que compromete los 4 cuadrantes. Angio-TAC tórax: imágenes en vidrio deslustrado con ocupación alveolar bilateral y difusa, sin foco de condensación. Sin lesiones vasculares pulmonares (Figura 3).
Con planteo de vasculitis sistémica con afectación pulmonar se inician bolos de metil-prednisolona 1 gr iv/día por 3 días y bolos de Ciclofosfamida 1 gr/mes durante 6 meses con excelente evolución clínico, paraclínica e imagenológica (Figura 4).

Figura 4: Caso clínico 2: TAC tórax control post bolo de Ciclofosfamida con franca mejoría imagenológica
A los tres meses del inicio de tratamiento se comprueba baciloscopia positiva (1 de 3) iniciándose tratamiento antituberculoso (isoniacida, rifampicina, pirazinamida y etambutol).
Actualmente finalizando tratamiento antituberculoso (isoniacida y rifampicina por cuatro meses), en plan de descenso de corticoides e inmunosupresores.
Caso Clínico 3
Sexo femenino, 64 años. AP: AR severa con secuelas articulares deformantes en manos, pies y columna cervical diagnosticada hace 34 años inicialmente tratada con metotrexate y sales de oro que se suspende hace 10 años, continuando en tratamiento con prednisona 10 mg vo/día y leflunamida 20 mg vo/día. Enfermedad de Sjogren. Fibrosis Pulmonar. Hipertensión arterial en tratamiento.
En los dos meses previos a la consulta incrementa la dosis de corticoides a 20mg/día por intensificación de los dolores articulares.
Consulta por cuadro de 1 semana de evolución dado por exacerbación de su disnea de esfuerzo habitual que se torna CF IV, tos y expectoración muco-purulenta. Fiebre y chuchos de frio. No dolor tipo puntada de lado. Del examen físico destacamos: Febril 38 °C axilar. PM: normocoloreadas. PP: FR 28rpm. Sat O2 92% en VEA. Estertores gruesos tipo “velcro” bibasales. Estertores subcrepitantes difusos bilaterales. OA: secuelas deformantes en regiones en manos y pies.
De la paraclínica se destaca: Hemograma: Hb 11 gr/dl, plaquetas 238.000/mm3, glóbulos blancos 15.940 neutrófilos 12.000. PCR 74. VES 67 mm3. Factor reumatoideo 210.
Radiografía de tórax: opacidad inhomogénea con broncograma aéreo en lóbulo medio derecho y lóbulo superior izquierdo.
Antígeno neumocóccico en orina negativo. Hemocultivos: sin desarrollo. PCR para TBC en expectoración positivo.
Con diagnóstico de TBC pulmonar se inicia tratamiento antituberculoso en base a isoniacida, rifampicina, pirazinamida y etambutol por 2 meses, continuando 4 meses con isoniacida y rifampicina.
Mejoría del cuadro respiratorio, ajustando el tratamiento corticoide de base.
Discusión
A la fecha, son varias las publicaciones a nivel internacional que vinculan las EAS con las complicaciones infecciosas, entre ellas la TBC.
Dentro de los factores de riesgo para el desarrollo de TBC se cuentan el compromiso inmune propio de la patología de base, el tratamiento inmunosupresor (destacándose, dosis de prednisona por encima de 7,5-10 mg /día, altas dosis de metilprednisolona y la ciclofosfamida)2)(6. Otros factores independientes de la dosis diaria de corticoides son la presencia de diabetes mellitus, IMC < 20Kg/m2, tabaquismo actual y presencia de enfermedad pulmonar obstructiva crónica (EPOC) 2
Presentamos tres casos de EAS (LES, vasculitis y AR) con elementos clínicos y paraclínicos de actividad que desarrollaron como complicación TBC
Si bien el compromiso pulmonar continua siendo el mas frecuente, como sucedió en los casos 2 y 3, se describe un aumento relativo en esta población de las formas extrapulmonares (25-30% según la serie) (3,7) destacándose la topografía osteoarticular, renal, partes blandas y neurológica como se observó en el caso 1.
Las pacientes 1 y 3 se encontraban bajo tratamiento corticoideo prolongado previo a la instalación del cuadro clínico, constituyendo este su principal factor de riesgo para el desarrollo de complicaciones infecciosas. Asimismo, pese al tratamiento recibido, ambos casos presentaban claros elementos de actividad de su enfermedad de base, lo cual constituye otro factor de riesgo para el desarrollo de estas complicaciones.
En el caso 2 la paciente desarrolla la infección tuberculosa posterior al inicio del tratamiento inmunosupresor (metilprednisolona y ciclofosfamida), siendo este su principal factor de riesgo para el desarrollo de la misma.
El diagnóstico diferencial entre infección y empuje de EAS en ocasiones es difícil. Ambas patologías pueden tener manifestaciones generales (fiebre, malestar y repercusión general), así como manifestaciones organoespecíficas 8 como compromiso neurológico en el caso 1 y respiratorio en los casos 2 y 3. Retrasos en el tratamiento de ambos procesos se relacionan con mayor morbimortalidad. La paraclínica es una de las principales herramientas diagnosticas a la hora de definir la terapéutica a instituir (1). En los tres casos se logro diagnostico de TBC, en el caso 1y 3 se logró el diagnóstico por técnicas de biología molecular (PCR para TBC en líquido cefalorraquídeo y expectoración respectivamente), mientras que en el caso 2 a través de la baciloscopía de esputo.
La técnica de PCR cuenta con una alta sensibilidad y especificidad siendo capaz de distinguir entre las diferentes especies dentro del complejo de las micobacterias con resultados en 2 horas, volviéndola una herramienta prometedora para el diagnóstico precoz 10.
De acuerdo a la revisión sistemática y de meta-análisis de la European Respiratory Society se analizan 18 estudios involucrando 4461 muestras. Concluyen que la sensibilidad del PCR para TBC varía en función del tipo de muestra. En punciones ganglionares la sensibilidad promedio fue de 83,1% frente al 81,2% del cultivo; en liquido cefalorraquídeo la misma es de 80,5 % frente a 62,8 % del cultivo; cayendo la sensibilidad en líquido pleural a 46,4% contra un 21,4%.11)(12)(13)(14
Todas las pacientes recibieron tratamiento antiTBC de acuerdo a pautas Nacionales de CHLA-EP 4, a la vez que se mantenía tratamiento inmunosupresor que posteriormente fue ajustado en dosis y fármaco.
Ante la mayor susceptibilidad de desarrollar infecciones oportunistas en pacientes con EAS destacamos la importancia de mantener un alto nivel de sospecha, así como el uso de herramientas paraclínicas que permitan detectar de manera precoz aquellos pacientes afectos de TBC latente.
Por el momento carecemos en el país de derivados purinicos purificados (PPD) por lo que debemos recurrir a nuevas técnicas de detección de TBC latente, entre las que se destaca técnicas inmunológicas (IGRAS - interferón gama reléase assay) como el Quantiferon. Entre los beneficios de esta nueva técnica destaca la mayor sensibilidad (90 - 98% vs 77- 90 % de sensibilidad del PPD 9), menor variabilidad en función del estado inmunológico del paciente, reproductibilidad, rapidez en obtener resultados.
Lamentablemente esta técnicas no están siempre disponibles, además de nos ser fácil su interpretación en los pacientes que presentan una EAS, lo que determina que en muchas oportunidades se realice la quimioprofilaxis empírica en aquellos pacientes que van a ser sometidos a tratamiento inmunosupresor.
Conclusiones
Si bien no es frecuente observar reactivación de TBC en pacientes con EAS bajo tratamiento inmunosupresor, su prevalencia se encuentra en ascenso.
Se reconocen factores de riesgo para su desarrollo, debiendo tener un alto nivel de sospecha para descartar diagnósticos diferenciales y sospechar las formas de presntación extrapulmonar, la necesidad de recurrir a técnicas diagnósticas de biología molecular para la confirmación de la infección.
Finalmente destacar la importancia de buscar TBC latente previo y durante el tratamiento inmunosupresor, a efectos de realizar quimioprofilaxis.















